8月28日,中國國家藥監局藥品審評中心(CDE)官網最新公示,阿斯利康(AZN.US)申報的acalabrutinib Maleate片上市申請已獲得受理。
智通財經APP獲悉,8月28日,中國國家藥監局藥品審評中心(CDE)官網最新公示,阿斯利康(AZN.US)申報的acalabrutinib Maleate片上市申請已獲得受理。公開資料顯示,acalabrutinib(通用名:阿可替尼膠囊)是一款布魯頓氏酪氨酸激酶(BTK)抑制劑,此前已經在中國獲批兩項適應症。根據阿斯利康官網管線信息,推測此次阿可替尼申報上市的新適應症可能是一線治療慢性淋巴細胞白血病(CLL)。
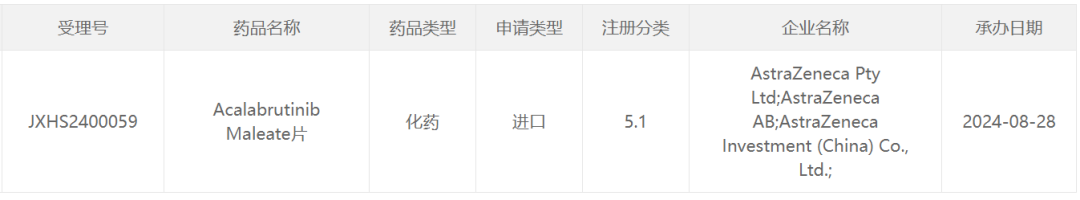
資料顯示,阿可替尼是新一代高選擇性原研BTK抑制劑,通過與BTK共價結合抑制其活性。在B細胞中,BTK信號導致B細胞增殖、轉運、趨化和粘附所需的途徑激活。在中國,阿可替尼於2023年3月首次獲批上市,用於治療既往至少接受過一種治療的成人套細胞淋巴瘤(MCL)患者;於2023年9月獲批第二項適應症,單藥適用於既往至少接受過一種治療的成人慢性淋巴細胞白血病(CLL)/小淋巴細胞淋巴瘤(SLL)患者。
