中國國家藥監局藥品審評中心(CDE)網站最新公示,翰森製藥(03692)第三代EGFR-TKI新藥甲磺酸阿美替尼片一項新適應症上市申請獲得受理。
智通財經APP獲悉,11月27日,中國國家藥監局藥品審評中心(CDE)網站最新公示,翰森製藥(03692)第三代EGFR-TKI新藥甲磺酸阿美替尼片一項新適應症上市申請獲得受理。公開資料顯示,這是阿美替尼片在中國提交的第五個適應症上市申請。
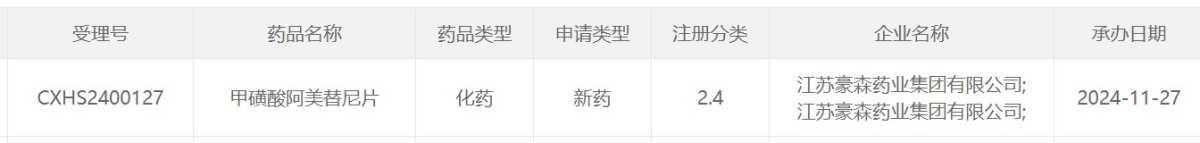
截圖來源:CDE官網
 今年10月22日,翰森製藥宣佈,一項阿美替尼片聯合化療作爲局部晚期(IIIB-IIIC期)或轉移性(IV期)EGFR突變非小細胞肺癌(NSCLC)患者的一線治療方案的3期註冊試驗AENEAS2達到了其主要終點即無進展生存期(PFS)。翰森製藥表示該試驗的詳細數據將在未來醫學會議上發佈及向監管機構遞交。由此推測,這可能爲本次阿美替尼申報上市的適應症。
今年10月22日,翰森製藥宣佈,一項阿美替尼片聯合化療作爲局部晚期(IIIB-IIIC期)或轉移性(IV期)EGFR突變非小細胞肺癌(NSCLC)患者的一線治療方案的3期註冊試驗AENEAS2達到了其主要終點即無進展生存期(PFS)。翰森製藥表示該試驗的詳細數據將在未來醫學會議上發佈及向監管機構遞交。由此推測,這可能爲本次阿美替尼申報上市的適應症。

 今年10月22日,翰森制药宣布,一项阿美替尼片联合化疗作为局部晚期(IIIB-IIIC期)或转移性(IV期)EGFR突变非小细胞肺癌(NSCLC)患者的一线治疗方案的3期注册试验AENEAS2达到了其主要终点即无进展生存期(PFS)。翰森制药表示该试验的详细数据将在未来医学会议上发布及向监管机构递交。由此推测,这可能为本次阿美替尼申报上市的适应症。
今年10月22日,翰森制药宣布,一项阿美替尼片联合化疗作为局部晚期(IIIB-IIIC期)或转移性(IV期)EGFR突变非小细胞肺癌(NSCLC)患者的一线治疗方案的3期注册试验AENEAS2达到了其主要终点即无进展生存期(PFS)。翰森制药表示该试验的详细数据将在未来医学会议上发布及向监管机构递交。由此推测,这可能为本次阿美替尼申报上市的适应症。