競争が白熱化していますか?
7月19日、国家薬品監視局の公式ウェブサイトによると、イーライリリーが申請したムフォンダ(テセルボリン注射液)の長期的な体重管理適応証が承認され、これは中国で承認された初の革新的医薬品である。
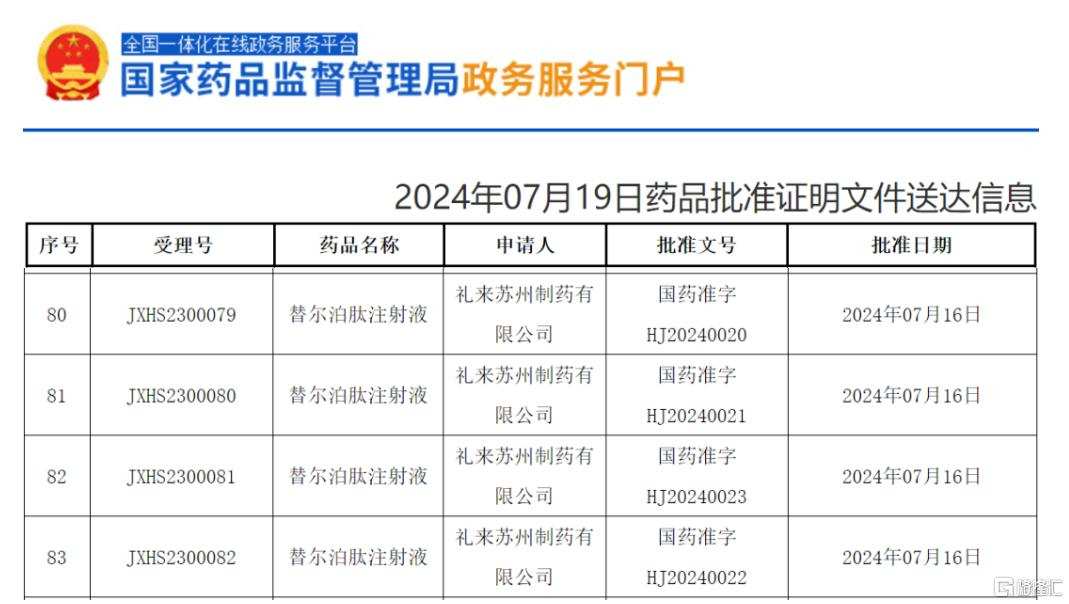
イーライリリーが最初に発表した件名によると、テセルボリン注射液は低カロリー食と運動が増えた状態で、1つ以上の体重関連合併症を有する超重患者の長期的な体重管理を改善するために使用されます。今年5月、テセルボリンは成人2型糖尿病患者の血糖コントロールに使用するために初めて承認されました。
以前、国家薬品監視局は6月に、ノボノルディスク社が開発したノルビジン(スメグルリン注射液)の中国国内での販売申請を承認しています。現時点で、減量分野の2つの人気製品は、中国で承認されています。
二大企業が中華の土地で競う
イーライリリーは、今回承認されたムフォンダ(テセルボリン注射液)が中国で長期的な体重管理で使用されることを明らかにしています。今年5月、テセルボリンは成人2型糖尿病患者の血糖コントロールに使用するために初めて承認されました。
テセルボリンは、グルコース依存性インクレチンポリペプチド(GIP)およびグルカゴン様ペプチド-1(GLP-1)受容体作動薬を1週間に1回注射するものです。テセルボリンは、食物摂取を減らし、食欲を調整してカロリー摂取量を減らし、体重を減らし、脂肪含量を減らすことで働きます。さらに、テセルボリンは脂質の利用を調節することも証明されています。
2022年5月、テセルボリンはアメリカ食品医薬品局(FDA)から2型糖尿病患者の血糖コントロール改善に承認を受けました(食事療法と運動を前提にして)。そして、2023年11月、この製品はBMI≥30kg/㎡の肥満(またはBMI≥27kg/㎡の重度の成人)の長期的な体重管理(低カロリー食と体力活動の増加を前提に)に譲るためのFDAの承認を受けました。テセルボリンはまた、素有「医薬業界のノーベル賞」と呼ばれるガレン賞の「最優秀医薬品賞」に2023年に入選しています。
従来から、イーライリリーとノボノルディスクは、減量の世界では2大企業として知られており、ノボノルディスクのスメグルリン注射液は中国市場で先行投資を行いました。
1月26日、ノボノルディスクのスメグルリン錠が国家薬品監督管理局によって承認され、6月25日、同局が長期的な体重管理用のノボノルディスクのスメグルリン注射液の国内販売申請を承認しました。
スメグルリンは、新しい長時間作用型GLP-1受容体作動薬の類似物です。この薬は、2型糖尿病治療において、膵臓β細胞のインスリン分泌を促進し、膵臓α細胞のグルカゴン分泌を抑制して血糖値を低下させます。肥満のある2型糖尿病患者の場合、この薬を使用すると、胃の排出を遅らせ、摂取エネルギーを減少させて体重を減らす効果が得られます。
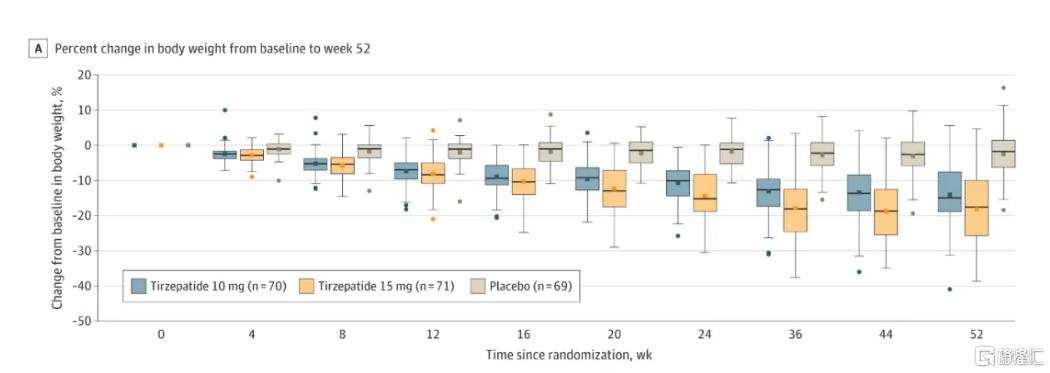
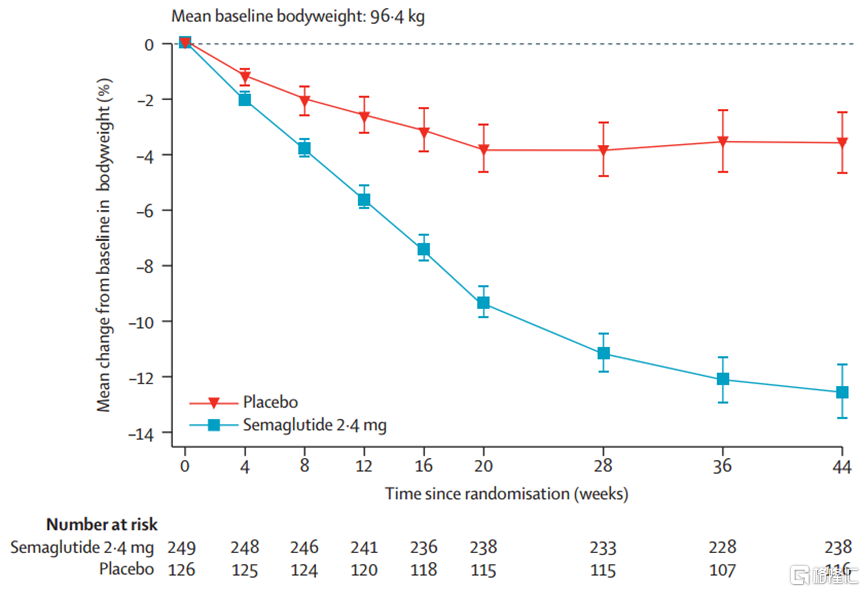
2つの製品の減量効果を比較すると、テセルボリンが勝っています。
イーライリリーの中国人群研究SURMOUNT-CNの結果によると、10mgの投与量を52週間(約1年)投与すると、13.6%の減量が得られ、15mgの投与量を52週間投与すると、17.5%の減量が得られます。スメグルリンSTEP 7試験には70%が中国人が含まれており、44週間(約10か月)のスメグルリン摂取で、12.1%の体重減少が実現しました。
減量製品市場が熱を帯びています。
注目すべきは、新しい減量薬が人々の生活を変え、従来の食事制限や運動を必要とせずに劇的に減量できることです。
関連機関によると、今後6年間、中国の糖尿病(および減量)薬市場規模は倍増し、230億ドル(約1700億人民元)以上になると予想されます。同時に、ゴールドマンサックスは、2030年までに、全体の減量薬市場は1000億ドル(約7200億元)に急増すると予測しています。
この背景を受けて、GLP-1減量薬は市場の新しいホットスポットとなっており、国内外の製薬企業が激しく競争しています。
2023年7月、華東医薬のリラルペプチド注射液(ルーパリド)、人会バイオのベナルペプチド注射液(フィスプメイ)が、肥満または超過応用症の販売許可申請を受けました。関係者によると、リラルペプチド注射液は、1000以上の大病院で入院販売が実現し、同社はオンラインプラットフォームおよびオフライン薬局の展開などに取り組んでいるとのことです。
甘李製薬が自社のGLP-1受容体刺激薬GZR18注射液の中国の肥満/過体重の人々に対するIb/IIa相臨床試験結果が35週間後に示され、GZR18治療を受けたGZR18 QW群において平均体重が基準値から17.8%減少しました。
hybio pharmaceuticalのチロシン脱ヨード原料薬はFDAのDMFに基づく登録番号を受け取りました。同様の製品が市場で競合している中、DMF登録登録を取得した企業と製品は顧客に優先的に考慮される可能性があります。
国投証券のアナリストは、国内の減量に対するイノベーティブな薬の競争優位性を見ると、開発進捗が早く、臨床的な減量データや安全性データが優れ、患者に依存性が高い製品が相対的な競争優位性を持っていると述べています。
患者の依存性を向上させることができる製品の場合、投与期間を延長したり、注射から経口摂取に最適化したりする企業は、減量などの慢性疾患の分野で相対的な優位性を得ることができる可能性があります。
編集/エミリー

