医療保険の優位性が際立っている。アリス社のアルコキシキニンの売上高は前半年に15.55億円に達し、2四半期の販売費用は前四半期に比べて減少している。現金残高は26億を超えている。
百済神洲は中国の革新的医薬品海外展開の輝かしい戦績を代表しているならば、アリスは国内での革新的医薬品の成長の秀でた存在である。百済神洲のゼブチニブの売上高は上半年に112.6億ドル、同期のアリスのアルコキシキニンは155.5ドルであり、両社とも今年自社が更新する30億ドル/人民元の目標を目指している。
アリスの比較増加は引き続き続いており、品質も向上しています。
第3世代EGFR-TKIのアルコキシキニンは医療保険によって支援されており、アリスは2四半期に引き続き2桁の成長を続け、販売費用は前四半期に比べて減少し、経営の質が著しく向上しています。
 8月20日には、同社が2024年半期報告書を発表し、当社は15.76億元の売上高を実現し、前年同期比で110.57%増加し、当社純利益は6.56億元で、前年同期比で214.82%増加しました。
8月20日には、同社が2024年半期報告書を発表し、当社は15.76億元の売上高を実現し、前年同期比で110.57%増加し、当社純利益は6.56億元で、前年同期比で214.82%増加しました。
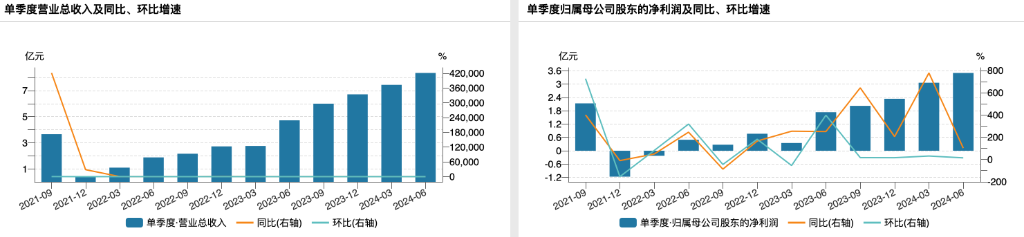
2四半期において、アリスは引き続き比較増加を維持しています。24Q2の当社の売上高は8.34億元で、前年同期比で76.56%増加し、前四半期比で12.2%増加しました。純利益は3.5億元で、前年同期比で101.73%増加し、前四半期比で14.39%増加しました。
売上が引き続き続くのは、2024年1月1日に新しい国家医療保険目録が公式に実施されたためです。同社の主力製品であるアルコキシキニンの二線、一線における非小細胞肺癌適応症が共に国家医療保険の払い戻し範囲に継続的に含まれており、今後半年間の売上増加を続けています。
特に注意すべきは、同社の営業活動によるキャッシュフローの純現金流は7.3億元で、前年同期比で293.73%増加し、純利益の成長速度を超えました。
報告期末までに、当社の現金および現金同等物は2.58億元、取引型金融資産(ストラクチャドデポジット)は23.42億元で、在庫現金は26億円を超えています。
現金の大幅な増加は、当社の中期的な配当に現金基盤をもたらします。
同時に、アリスはすべての株主に対して、現金配当を10株あたり2.5元(税込み)支払うことを計画しており、配当総額は1.125億元で、株式配当率は17.15%となる予定です。これは23年間の年次報告書に続いて初めての中期配当となります。革新的な医薬品企業が安定的に利益を上げた後の配当は、投資家にとって重要な投資リターン指標となっています。
現金配当は、同社の経営に悪影響を与えなかった。声明期末時点で、同社の負債率は約9%で、長期および短期の借入金はどちらもありません。したがって、当期の財務費用はマイナス1.5億元でした。
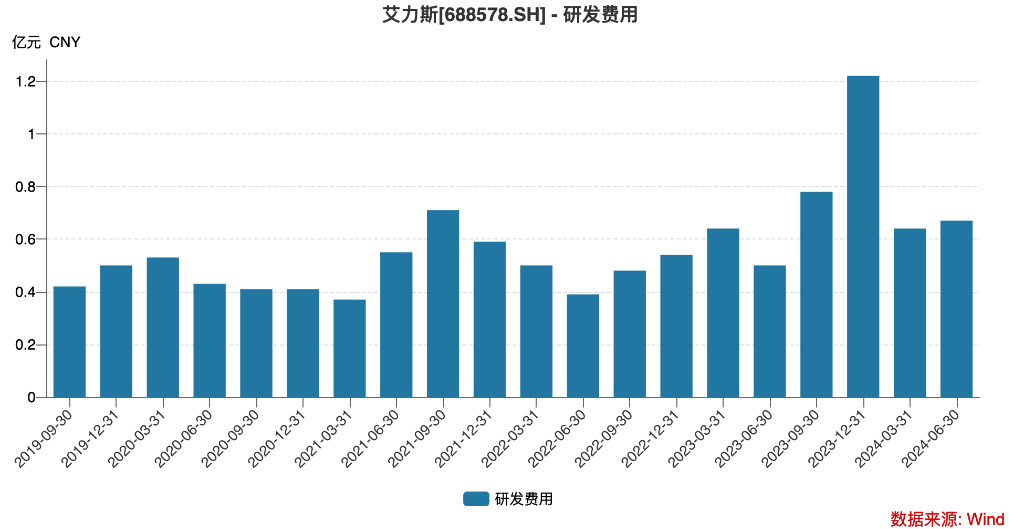
研究開発については、当社は当期投資額を1.31億元に投資し、前年同期比でわずかに-0.74%減少し、売上高の大幅な増加により、研究開発/売上高は前年同期比で9.33%減少して8.33%になりました。

売上費用面では、アリスは優れたパフォーマンスを発揮しています。販売の環境が前四半期に比べて2桁の成長を続けている中、同社の販売費用は2四半期で30.9億元で、前四半期に比べて1.34%低下しています。つまり、医療保険は革新的医薬品の大口放出に対して前向きな意味を持っています。
より多くのパイプラインと適応症があり、アルコキシキニンにはまだ成長の余地があります。
肺がん領域においては、第3世代EGFR-TKIの治療潜在性は、EGFR感受性突然変異NSCLC一次、EGFR T790M突然変異陽性NSCLC二次の適応症にとどまりません。現在、アリスは伏美替尼の臨床的な潜在性を急速に掘り下げており、その臨床的な適用範囲を拡大するために努力しています。

8月16日、中国の医薬品臨床試験登録および情報公開プラットフォームによると、アリスは第III相臨床試験を登録しました。EGFR感受性突然変異陽性の非扁平上皮小細胞肺癌(NSCLC)の脳転移を有する患者を対象に、伏美替尼とプラチナ含有二次化学療法の有効性と安全性を比較するためのものです。
2024年1月、伏美替尼は20外顕子挿入突然変異NSCLC一次治療適応症として国家薬品監督管理局薬品審査中心突破的治療品種リストに掲載されました。アリスがArriVentと協力している伏美替尼は、グローバル、多元中心、III相臨床試験で20外顕子挿入突然変異一次治療適応症に適用され、順調に進展しています。
また、アリセス製剤は、III相登録試験後の補助治療適応についてもスムーズに進展し、上半期に患者登録を完了しました。EGFRまたはHER2変異を有する進行期NSCLC患者に使用されます。フォセチニブとFAK小分子阻害剤IN10018を併用した進行期NSCLCの治療。フォセチニブと抗体薬物複合体(ADC)RC108の併用による晩期NSCLCの治療。

ただし、第三世代EGFR-TKIの競争はますます激化しており、今年上半期には2つの新製品が市場投入されたため、現時点で承認されている適応症は第2線のNSCLCであるが、間違いなく第3世代EGFR-TKI市場にはより多くの参入者が現れ、特に医療保険に加入した後。
ただし、アリセスは新製品の臨床試験も迅速に進めています。
早期のパイプライン製品の開発では、2024年3月に、同社が全世界的な知的財産権を持つKRAS G12D選択的阻害剤である注射用AST2169リポソームの第I相臨床試験が承認されました。 KRAS G12D変異体は、非小細胞肺癌、大腸癌、膵臓癌などのさまざまなタイプの癌で見られるKRAS変異体の一般的なサブタイプであり、現時点ではKRAS G12D阻害剤が承認されていません。
外部協力では、同社は新しいEGFR経口小分子阻害剤AST2303(ABK3376)のIND申請を提出しました。同製品は、EGFR C797S突然変異を有する進行期NSCLC成人患者の治療に使用されます。

前臨床段階では、同社には現在、多数の製品が開発中です。
アリセスは2四半期で素晴らしい財務報告書を提出しました。フォセチニブの1年間の販売額が30億を超える可能性はまったく疑いの余地がありません。市場が期待する次の問題は、ピーク時の販売額が50億に達するかどうかです。


 8月20日晚间,公司发布2024年半年报,期内公司实现营收15.76亿元,同比增长110.57%;归母净利润6.56亿元,同比增长214.82%。
8月20日晚间,公司发布2024年半年报,期内公司实现营收15.76亿元,同比增长110.57%;归母净利润6.56亿元,同比增长214.82%。