現在、双抗の分野の熱気と活気は急速に高まっており、グローバルの革新的医薬品業界の新しい最前線となっており、多国籍医薬品企業が一斉に買い物をしており、潜在的な双抗パイプラインを積極的に探し出し投資しています。
グロインモニターの統計によると、2024年の第1〜第3四半期までに、グローバルの医薬品企業は双抗医薬品分野における取引活動が非常に活発であり、総額31件の取引が達成されました。この数字は、過去3年間のいずれの年の年間取引量よりも多く、双抗医薬品がグローバル医薬市場での地位と影響力が急速に上昇していることを示しています。
そのうち、11月だけで、双抗/三抗医薬品に関する5件の大型BD取引が発生し、高額の協力金額が双抗競技の巨大な事業価値を示しています。
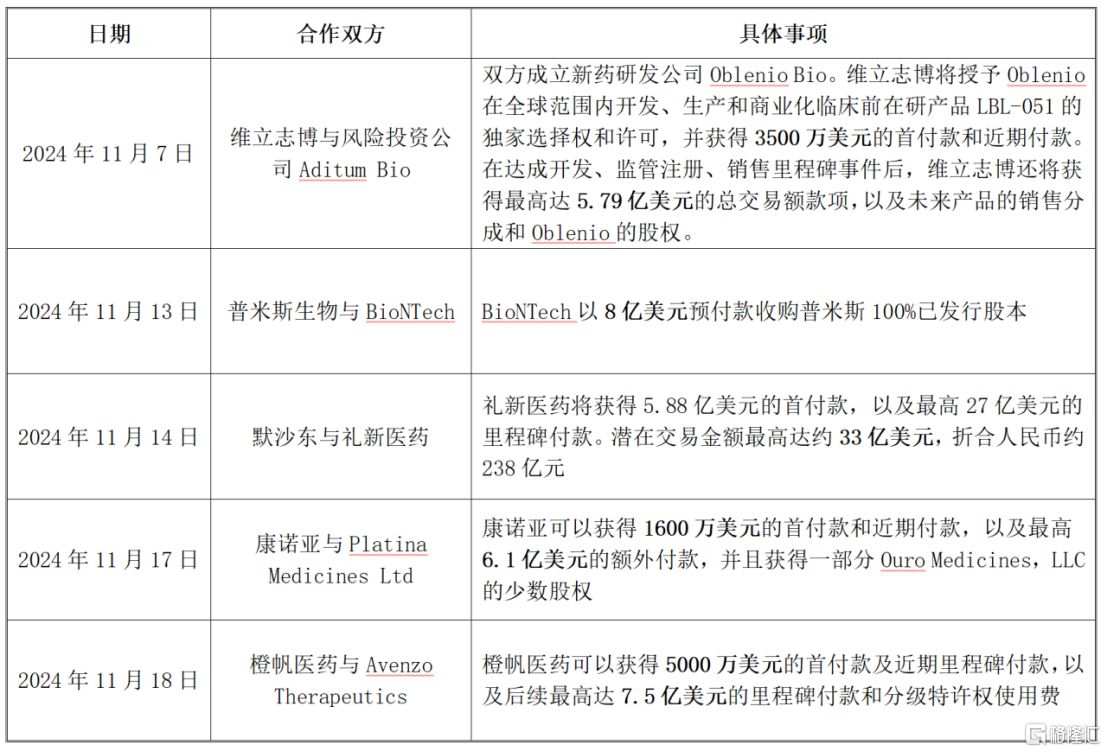
 情報提供元: 格隆汇はネットワーク上で公開された情報を整理しました。
情報提供元: 格隆汇はネットワーク上で公開された情報を整理しました。
なぜ資本や世界中の大手医薬品企業が双抗医薬品をここまで支持しているのでしょうか?
がん免疫療法の進化の経緯から見ると、PD-1モノクローナル抗体を代表とする前代のがん免疫療法が約20%の客観的な緩和率を達成できるものの、がん微環境の複雑性と変異性のために、その効果は一般的に限られており持続的ではありません。
このように、双抗を代表とする次世代のがん免疫療法が登場し、より高い治療潜力を示しています。この段階では、免疫チェックポイント阻害剤が化学療法または抗血管新生薬と併用され、客観的な緩和率が40%から50%に向上しています。さらに、現在、より高い客観的緩和率を達成するために、4-1BBとPD-L1の組み合わせ、LAG3とPD-1の組み合わせなど、新たなターゲットを持ち将来性のある組み合わせ療法が登場し、多様な免疫経路をシステム的に標的とし、免疫系を包括的に活性化させ、がん免疫療法の将来の方向を示唆しています。フォスターサリバンのデータによると、免疫療法は2030年には世界のがん治療市場の約半分を占めることが期待されています。
当然、このビジネス価値の表現は、市場規模の拡大にも現れています。PharmaVivienによると、2023年のグローバル双対抗薬市場規模はすでに88億ドルに達し、前年比50%増加し、双対抗薬市場のポテンシャルと活力をさらに裏付けています。
このような市場環境の中で、投資家は双対抗領域への関心も高まっており、その中には注目に値する投資機会も多く存在しています。
最近、百済神州が香港株取引所に上場申請を行ったことは、注目に値するケースと言えるでしょう。
現在の双対抗レースの熱気の中、フォースターサリバンのデータによると、百済神州の4つの主要製品(双対抗LBL-024、LBL-034、LBL-033、および単一抗体LBL-007)は、製品設計だけでなく臨床研究の進捗においても革新性を示しており、それぞれの薬物カテゴリーまたは同一標的においても世界的に先駆けています。パイプラインの革新性と先見性により、百済神州は次世代のがん免疫療法の先駆者となっています。
百済神州が香港株取引所に上場するタイミングはまさに適切であり、会社自体に資本市場の注目を引き付けると同時に、投資家にとってこの成長分野を把握するための窓口を提供しています。
差別化された標的の探求により、グローバルなFIC/BICが革新的なハードパワーを示す
グローバルな創新医薬品研究開発分野では、企業が成功するためには、そのカードが非常に強い必要があります-すなわち、製品の革新性と臨床応用の潜在性を見る必要があります。
創立以来、百済神州はがん、自己免疫疾患、およびその他の重大な疾病に関する中国およびグローバルの未解決メディカルニーズに応えることに取り組んでおり、差別化された革新と広範囲にわたる治療領域のカバレッジにより、双対抗、単一抗体、ADCなど多くの医薬品分野で布石を打ち、それらはすべてグローバルな商業権を持ち、多様な成長パスを早期に確立しています。
目前、ブロードコムは、がんに対する3つの単一抗体、4つの二重抗体、2つのADC、および1つの二重特異性融合タンパク質、自己免疫疾患に対する1つの二重特異性融合タンパク質、および1つの三重特異性抗体を含む、12個の候補薬品を持つ製品パイプラインを確立しています。そのうち6つの製品は臨床段階に進んでおり、核心製品LBL-024および主要製品LBL-034、LBL-033、LBL-007を含み、研究開発の進捗は世界トップレベルであり、革新的医薬品開発分野での強力な実力を示しています。
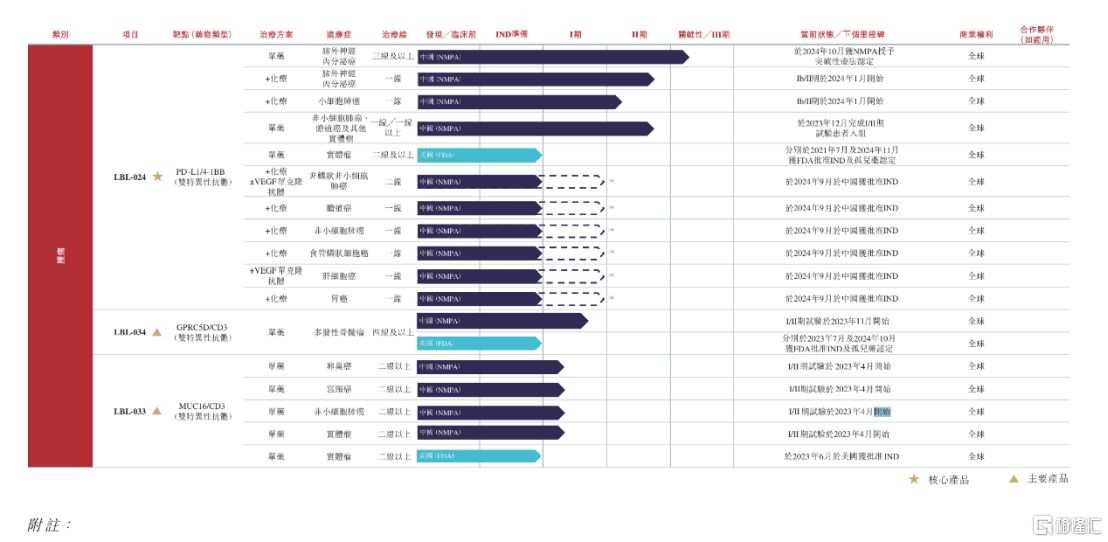

資料来源:维立志博招股书
例えば、二重抗体領域では、ブロードコムの核心製品LBL-024は、PD-L1と4-1BBの二重抗体であり、世界初の4-1BB標的免疫療法となる可能性があります。
グローバルで初のPD-1/PD-L1免疫チェックポイント阻害剤を代表とするがん免疫療法の最初の波では、単剤治療でも客観的な緩和率は20%にすぎませんでした。LBL-024は、双方向性戦略を通じて、これら2つの経路の協力効果を利用して、強力な治療効果とコントロール可能な毒性のバランスを実現し、より安全かつ効果的な治療法を提供し、PD-1/L1免疫療法に理想的な補完となっています。
ここで注目すべきは、4-1BBは共刺激刺激剤として、単一抗体の開発道路は重大な挑戦が多いということです、特に安全性の問題があります。臨床データによれば、LBL-024は、単剤または化学療法との併用治療で、どちらも優れた安全性を示しています。単剤療法のI/II相試験では、175人の患者(II相111人)が0.2mg/kgから25mg/kgの大量投与療法を3週ごとに1回受ける中、投与制限性の毒性は観察されなかった。ほとんどの有害事象は1〜2度であり、管理可能でした。また、化学療法との併用療法のIb/II相試験では、2024年9月30日時点で、意図入試入組肺外神経内分泌腫瘍患者47名が6mg/kg、10mg/kg、15mg/kgの投与量を受け、最大耐用量に達していない15mg/kgの高用量でも投与制限性毒性が観察されませんでした。
その他、単剤療法で得られた効果のデータも励みとなります。例えば、2024年9月30日時点で、二次/三次以上の肺外神経内分泌腫瘍の評価可能患者45名において、一部の緩和を達成した15名、疾患の安定を達成した8名があり、客観的緩和率は33.3%であり、疾患制御率は51.1%でした。肺外神経内分泌癌に対しては、ブロードコムは核心となる臨床試験を起動しています。
同时、4-1BBおよびPD-L1の広範な発現により、多くの適応症で成薬の潜在性を持ち、その適用範囲は広く、多彩な実体腫瘍にまで拡張される。以前のフォロストサリバンのデータによると、4-1BB抗体の主な適応症の症例数は年々増加し、2016年の971.7万例から2020年の1063.4万例に増加した。
現在、ウェルバイリーコープは遅発性肺外神経内分泌癌、小細胞肺癌、胆道癌、非小細胞肺癌などの他の実体腫瘍の治療を対象としたLBL-024の臨床研究を行っており、食道扁平上皮癌、胃癌、肝細胞癌など、さらに多くのがん適応症領域に拡大する予定です。
わずか3年足らずで、LBL-024は初のヒト実験から肺外神経内分泌癌に対する単独の重要な臨床試験に進み、優れた効果と安全性を示し、グローバルで初めての4-1BB標的候補薬となり、その適応症の初めての承認薬品となる可能性があります。LBL-024は既にNMPAから肺外神経内分泌癌の治療後の究極的な治療法認定を受け、米国FDAから神経内分泌癌の孤児薬認定を受けています。
もう1つの主力製品LBL-034は、グローバルで第2位のGPRC5DおよびCD3 T細胞エンゲージャーです。
最新の臨床進展によると、LBL-034はNMPAおよび米国FDAからIND承認を受け、中国で難治性多発性骨髄腫のI/II相試験が行われています。
2024年11月22日時点で、治療400μg/kgにより、LBL-034の客観的奏効率(ORR)は88.9%に達し、VGPR(非常に良好な奏効)またはそれ以上の効果比率が66.7%となり、治療800μg/kgでのORRは100.0%に達しました。また、グローバルで唯一承認されたGPRC5D/CD3二重抗体であるジョンソンエンドジョンソンのTALVEY(タキユトキシマブ)の公開された臨床データに比べ、800μg/kgの多発性骨髄腫患者においてVGPRまたはそれ以上の効果を達成した割合は52%です。LBL-034はより優れた効果を示しました。この結果はLBL-034の潜在性を証明するだけでなく、将来の市場競争の基盤を築きました。ジョンソンの売上予測によると、TALVEYの世界のピーク年間売り上げは50億ドルに達するでしょう。
このように、LBL-034が今後スムーズに臨床試験を進めて商品化に成功すれば、より優れた効果と臨床データにより、市場で迅速に支持され、TALVEYを上回る売り上げを達成する可能性があります。
また、フォロストサリバンのデータによると、もう1つのCD3 T細胞エンゲージャーLBL-033は、世界で唯一の2つの早期臨床段階に進んだMUC16/CD3二重抗体の1つで、以前の非臨床および初期臨床研究では、強力な抗腫瘍活性と制御可能な安全性が示されていました。現在、LBL-033はNMPAおよびFDAからIND承認を受け、中国で単剤治療の晩期実体腫瘍のI/II相臨床研究が実施されています。
そして、モノクローナル抗体領域では、フォスターサリバンのデータによると、百济神州のLBL-007は、世界でトップ3にランクインするLAG3を標的とするモノクローナル抗体の1つであり、同じ種類の抗体の中で鼻咽癌に有効と確認された最初の抗体でもあり、臨床試験の適応症数も同類製品の中でトップです。
百济神州のLBL-007は、現在、中国およびグローバルで鼻咽癌以外にも広範囲にわたる癌症に対する第II相臨床試験を実施中であり、非小細胞肺がん、大腸がん、頭頸部扁平上皮がん、食道扁平上皮がんなどに広く適用されています。
全体として、「世界初」「世界トップ3」などのリーダーシップの称号が多数あることから、百济神州の薬物開発における前向きな姿勢と革新能力が示されています。
さらに、これらの候補医薬品が臨床試験で示した優れた治療効果は、会社が患者のニーズを深く理解していることだけでなく、これらのニーズを実行可能な治療法に変える能力も証明しています。
真の源泉からの革新的な研究開発能力を持ち、業界の信頼と支持を集めています。
もちろん、百済神州の製品パイプラインがこのように革新的である重要な要因の1つは、真の源泉から革新的な研究開発能力を持っていることです。内部と外部の2つの視点から探ってみましょう。
内部から見ると、百済神州は、フルプロセスの研究開発リンクと包括的な開発能力を持ち、複数の特許技術プラットフォームを開発しています。これにより、会社は医薬品の開発プロセスで成功率を著しく向上させることができます。
これらのプラットフォームには、LeadsBodyTM(CD3 T-cell engager platform)、X-bodyTM(4-1BB engager platform)および他のいくつかのバイスペシフィック抗体および融合蛋白プラットフォームが含まれており、さまざまなターゲット、作用機序、および医薬品タイプに継続的に医薬品の革新を行い、多くの疾患領域に適用し、会社に持続的な成長動力を提供しています。
例えば、LeadsBodyTMプラットフォームの利点は、簡単に3つの点にまとめることができます。まず、腫瘍関連抗原とCD3結合領域の比率と親和性を最適化し、T細胞エンゲージャーの作用を腫瘍部位に誘導し、オフターゲット毒性を低下させることができます。次に、このプラットフォームは構造の最適化により、T細胞を誘導して標的細胞を効果的に殺し、細胞因子の分泌を減少させることができます。最後に、体外および体内研究では、このプラットフォームによって開発されたT細胞エンゲージャーは持続的な抗腫瘍効果を示し、誘導されるT細胞の減少が少ないことが示されています。LBL-034とLBL-033の優れた臨床データは、LeadsBodyプラットフォームが強力なCD3 T細胞エンゲージャーを開発する上で優れていることを証明しています。
一方、X-bodyTMプラットフォームは、最先端の抗体工学技術を用いて腫瘍関連性抗原と4-1BBの間の親和性をバランスよく保ち、腫瘍部位と腫瘍関連性抗原が結合した場合にのみ4-1BB受容体の連結と活性化を促進し、腫瘤環境での4-1BBの活性化を促進します。このユニークな分子構造は腫瘤環境における免疫応答を強化し、全身毒性のリスクを低減することができます。会社の中核製品であるLBL-024は、X-bodyプラットフォームに基づくものです。
さらに、会社のその他の技術プラットフォームは、世界的に競争力のあるターゲットに対して一連の薬物タイプの抗体ベースの候補製品をデザインすることができます。一般的な軽鎖二特異性抗体、二機能融合蛋白質、ADCなど、創新的な分子工学技術を活用して、二重機能の特定用途医薬品を作り出し、腫瘍細胞に精密に標的を絞ることで全身の副作用を軽減できます。これにより、会社のグローバルな創新医薬市場におけるリーダーシップ地位をさらに強化することができます。
内部のイノベーション能力と技術プラットフォームの強力な力を活かし、グローバルに満足されていない治療ニーズに焦点を当てることで、维立志博は全体として、新たな次元を付加するとともに、より多くの重い疾患に研究範囲を拡大する計画を立てました。これにより、市場の変化により良く対応でき、業界の新しいトレンドを把握しやすくなり、グローバルな創新医薬市場でのリーダーシップ地位を維持できるようになります。
外部から見ると、グローバルに競争力のある製品パイプラインを持つ维立志博は、世界中の有名な医薬品企業とのBDパートナーシップを通じて、グローバルな価値体系を拡大し、長期的に持続可能なビジネスモデルを築いています。これらのパートナーシップは、会社のイノベーション研究開発力が業界内で認められ、後のグローバル市場での展開と商業化に道筋をつけました。
例えば、维立志博と百済神州との協力はその典型的な例です。
维立志博は百済神州に対して、グレーターチャイナ地域外でLBL-007の独占的な開発、製造、商業化のライセンスを与え、両社は大がん種に対するLBL-007の臨床開発および商業化を共同で行い、契約額は7.72億米ドルの前払い金およびマイルストーンペイメントに加え、2桁の割合のグローバル販売分配を行います。この協力関係は、百済神州の薬物開発および商業化における豊富な経験と販売チャネルを活用し、LBL-007のグローバル登録および上市プロセスを加速し、维立志博の革新的な成果をグローバルに展開するための堅固な基盤を築くことが期待されています。
さらに、最近のTCE(T cell-engager)出海の熱い環境の中で、维立志博はAditum Bioと共同で新薬研究会社Oblenio Bioを設立し、LBL-051(CD19/BCMA/CD3 T cell engager)のグローバル開発および商業化に合意し、総額6.14億米ドルの金銭及びグローバル販売分配の中程度の2桁割合に加え、新会社の株式を提供しました。その後の国際化の道筋が明確になっています。
内部の革新能力と戦略的なグローバル協力により、ウィドジーボーは自社の革新的な研究開発能力を強化し続け、企業のグローバル革新医薬分野での影響力を高めると同時に、さらなる成長機会と市場競争力をもたらしています。
結論
現在の革新医薬品の研究開発では、標的同質化が業界内で普遍的な課題となっています。この状況に直面して、革新薬企業は長期的な市場競争力と持続可能な発展を確保するために差別化戦略を模索する必要があります。
ウィドジーボーはLBL-024、LBL-034、LBL-033、LBL-007などの差別化薬剤を掌握しており、革新的な先導的優位性は言うまでもありません。これらの薬剤の革新性は、標的の選択だけでなく、独自の作用メカニズムや治療潜在性にも表れています。
これらの製品優位性による独自の市場ポジショニングと成長潜力により、ウィドジーボーの香港株上場は多くの市場の関心を集め、全く新しい発展段階に進むことが期待されています。


 资料来源:格隆汇根据网络公开信息整理
资料来源:格隆汇根据网络公开信息整理