| 藥物濫用,或NIDA,以進一步評估TRV734對OUD的管理,NIDA於2019年12月啓動了一項關於這一適應症的概念驗證研究。2021年6月,我們宣佈因全球新冠肺炎疫情而暫停的研究重新開始招募患者。我們打算繼續將我們對TRV734的努力集中在確保這一資產的開發和商業化合作夥伴上。 |
我們的產品和流水線
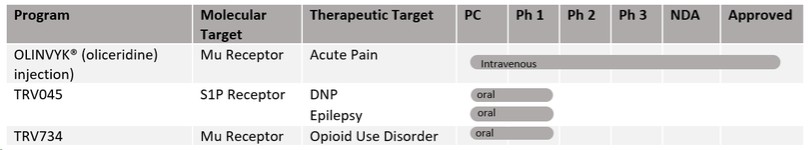
奧林維克®(奧利塞定)注射劑
OLINVYK是一種G蛋白偏向的MOR配體,被批准用於成人的急性疼痛,這種疼痛足夠嚴重,需要靜脈注射阿片類止痛劑,而且對那些缺乏替代治療的人來說。它是一種具有新穎作用機制的NCE。
疼痛治療方案
根據2021年IQVIA的數據,過去三年平均使用了約16500萬單位的靜脈阿片類藥物。傳統的靜脈注射阿片類鎮痛劑,如嗎啡、芬太尼和氫嗎啡酮,已成爲術後即刻疼痛控制方案的核心成分。傳統阿片類激動劑的有效性受到嚴重劑量依賴性副作用的限制,如呼吸抑制、噁心、嘔吐、便秘和鎮靜,這些副作用可因活性代謝物的積累和腎功能受損患者腎臟清除量的降低而加劇。傳統靜脈注射阿片類藥物的這些缺點在某些臨床實踐情況下給醫療保健提供者帶來了巨大的挑戰。
可注射非阿片類鎮痛劑通常與靜脈注射阿片類藥物一起用於多模式手術後疼痛治療。然而,這些藥物,如靜脈注射非類固醇抗炎藥,或非類固醇抗炎藥,或靜脈注射對乙酰氨基酚,或局部麻醉藥,如布比卡因,都有自己的潛在心血管、肝臟和胃腸道副作用。此外,在許多患者中,這些非阿片類止痛藥都不能作爲單一療法提供足夠的療效來管理嚴重的急性疼痛。
我們認爲,OLINVYk解決了一個重要的未得到滿足的需求,即具有差異化的安全性、耐受性和PK/PD特徵的高效靜脈注射阿片類止痛劑。OLINVYk提供靜脈阿片類藥物療效,中位起效時間爲1-3分鐘,對於腎損害患者不需要調整劑量,腎損害患者是一個具有重大醫療併發症的龐大患者群體。
OLINVYk於2020年8月被FDA批准用於團注和患者自控鎮痛(PCA),我們在2021年第一季度啓動了OLINVYk的商業推出。DEA已將奧立卡定歸類爲附表II管制物質。與其他阿片類藥物一樣,OLINVYk的標籤上也包含一個「盒裝」警告和重要的安全信息。請訪問www.olinvyk.com查看處方信息以及重要的安全信息和盒裝警告。
OLINVYk VOLITION批准後研究
2023年,我們公佈了VOLITION研究的OLINVYk數據,這是一項由203名患者組成的真實世界、開放標籤、多站點研究,由克利夫蘭診所和維克森林浸信會健康醫療中心的臨床結果研究專家領導。 OLINVYk在術後護理期間作爲一線鎮痛藥給藥,負荷劑量爲1.5毫克
5